Halo teman-teman semua, informasi berikut ini akan membahas mengenai rumus molekul senyawa beserta contoh soal molekul senyawa.
Tujuannya adalah agar teman-teman semua bisa semakin memahami apa itu molekul senyawa dan bagaimana cara menyelesaikan contoh soal molekul senyawa.
Rumus molekul senyawa menyatakan jumlah atom dari berbagai macam unsur yang kemudian atom tersebut menyusun satu molekul senyawa. Rumus ini menyatakan molekul dari suatu zat.
Untuk penjelasan selengkapnya, yuk kita baca informasi di bawah ini!
Rumus Kimia Molekul Senyawa

Seperti yang sudah dijelaskan di atas bahwa rumus molekul senyawa menyatakan molekul dari suatu zat.
Begini contohnya:
Di dalam reaksi fotosintesis, terdapat senyawa glukosa dengan rumus C6H12O6.
C6H12O6 artinya glukosa tersusun dari rangkaian berikut ini:
Baca juga: Gambar Molekul Senyawa
- 6 atom karbon
- 12 atom hidrogen
- 6 atom oksigen
Penggunaan rumus atau molekul senyawa penting dalam industri farmasi dan kimia karena melibatkan bahan-bahan kimia juga menjadi suatu zat yang baru.
Penjelasan rumus kimia molekul senyawa

Rumus kimia molekul senyawa menunjukkan jumlah atom di dalam suatu senyawa yang menyusun suatu zat.
Rumusnya ditentukan oleh persentase unsur dari senyawa itu sendiri.
Berikut ini rumus molekul senyawa jika diketahui persentase unsur-unsurnya:
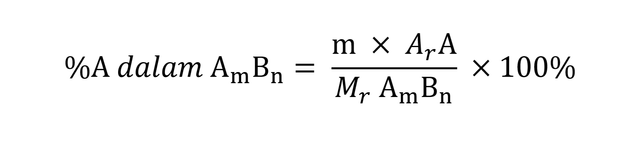
Keterangan:
- Ar = massa atom relatif
- Mr = massa molekul relatif
Berikut ini rumus molekul senyawa jika diketahui massa senyawa atau unsur-unsurnya:
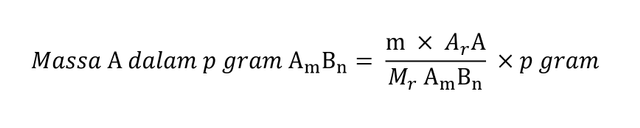
Keterangan:
p gram = masa total AmBn
Contoh Soal Molekul Senyawa
Berikut ini beberapa contoh soal molekul senyawa yang bisa teman-teman gunakan untuk belajar sehingga lebih memahami bagaimana cara menggunakan rumus molekul senyawa:
Contoh soal molekul senyawa 1
Tuliskan rumus molekul senyawa berikut jika diketahui senyawa tersebut mengandung 80% unsur karbon dan 20% unsur hidrogen!
Diketahui Mr senyawa 30, Ar karbon adalah 12, dan Ar H adalah 1.
Penyelesaian:
1. Jumlah atom karbon
%C = ((n x Ar C) / Mr) x 100%
80% = n x 12 x 100% / 30
n = (80% x 30) / (100% x 12)
n = 2
Baca juga: Menghitung Penjumlahan Pecahan
2. Jumlah atom hidrogen
%H = ((n x Ar H) / Mr) x 100%
20% = m x 1 x 100% / 30
m = (20% x 30) / (100% x 1)
m = 6
Jadi, rumus molekul senyawa tersebut adalah C2H6.
Contoh soal molekul senyawa 2
Tentukan rumus molekul senyawa itu!
Suatu senyawa disusun dari 0,18 gram karbon, 0,03 gram hidrogen, dan 0,08 gram oksigen.
Massa molekul relatif senyawa tersebut adalah 58 dengan Ar H = 1, Ar C = 12, dan Ar O = 16.
Penyelesaian:
1. Rumus molekul senyawa dimisalkan dengan CiHjOk.
Massa senyawa = massa C + massa H + massa O
Massa senyawa = 0,18 + 0,03 + 0,08
Baca juga: Mencari Determinan Matriks 2×2
Massa senyawa = 0,29 gram
2. Jumlah atom karbon
Massa C = ((i x Ar C) / Mr) x massa senyawa
0,18 = i x 12 x 0,29 / 58
i = 3
3. Jumlah atom hidrogen
Massa H = ((j x Ar H) / Mr) x massa senyawa
Baca juga: Menghitung Perkalian Pecahan
0,03 = j x 1 x 0,29 / 58
j = 6
4. Jumlah atom oksigen
Massa O = ((k x Ar O) / Mr) x massa senyawa
0,08 = k x 16 x 0,29 / 58
k = 1
Jadi, rumus molekul senyawa tersebut adalah C3H6O.
Contoh soal molekul senyawa 3

Jika diketahui rumus empiris suatu senyawa adalah CH4 (Ar C = 12, Ar H = 1) dan masa molekul relatif(Mr) adalah 32.
Tentukanah rumus molekul senyawa tersebut ?
Penyelesaian:
1. Menentukan Rumus Empiris
Rumus Empiris : CH4
Baca juga: Bimbel Intensif SBMPTN
2. Menentukan massa molekul relatif senyawa
Mr = 32
3. Menentukan nilai n
Mr rumus empiris x n = Mr rumus molekul
(Ar C + 4 Ar H) x n = 32
(12 + 4) x n = 32
Baca juga: Mencari Determinan Matriks 3×3
16n = 32
n = 2
4. Rumus Molekul = (Rumus Empiris) x n
Rumus molekul = (CH4) x 2 = C2H8
Jadi, rumus molekul yang didapat adalah C2H8
Itu dia penjelasan contoh soal molekul senyawa kali ini untuk Sahabat Latis semua. Semoga mudah dipahami dan bermanfaat ya!
Baca juga: Bimbel PTN
Itu dia penjelasan singkat yang bisa kami sampaikan, jika teman-teman masih kurang paham, coba ulangi membaca penjelasan di atas dan kunjungi website kami untuk membaca artikel lainnya terkait materi yang sama di www.tutorindonesia.co.id.
Jika kalian sedang mencari tutor terbaik atau guru berpengalaman untuk membantu meningkatkan nilai di sekolah atau belajar jadi lebih mudah, daftarkan diri kalian sekarang juga les privat bersama kami di Tutor Indonesia dari tim latis education.
Atau datangkan guru berkualitas kami ke rumah, kalian bisa melihat review asli dari customer kami di google sebagai kategori best management, best quality tutor, dan best system.
Kapan lagi, kan, mendatangkan guru terbaik dengan pelayanan maksimal?
Baca juga: Rumus Pembagian Pecahan
Coba gratis sekarang juga dengan menghubungi kami di nomor 6287-7816-09961 atau hubungi head office kami di 021-7784-4897 setiap hari senin sampai jumat pukul 9 pagi hingga 5 sore.
Jika kalian ingin berkunjung langsung ke kantor pusat kami, kunjungi alamat berikut ini:
Kantor Ocean Terrace Residence Blok E1 Nomor 1, Jalan Tole Iskandar, Tirtajaya, Kecamatan Sukmajaya, Kota Depok, Jawa Barat.
Kami tunggu kedatangan kalian semua, ya! ^^
Referensi:
https://kumparan.com/berita-unik/rumus-molekul-senyawa-penjelasan-dan-contoh-soal-1vtwzlutPX4/full
https://www.kontensekolah.com/2019/07/contoh-soal-rumus-molekul-beserta.html